Qu’est-ce que l’ozone ? Comment cela se produit-il ?
Le numéro CAS de l’ozone est 10028-15-6. L’ozone est un oxydant puissant qui peut entrer dans de nombreuses réactions chimiques avec des composés organiques et inorganiques. Le potentiel d’oxydation de l’ozone est supérieur à celui de nombreux produits chimiques connus. Alors que le potentiel d’oxydation du peroxyde d’hydrogène couramment utilisé est de 1,77 eV, l’ozone vient après le fluor avec 2,07 eV par 3,06 eV et les radicaux hydroxyles par 2,80 eV. L’ozone, qui a un potentiel d’oxydation très élevé, est également un stérile efficace. De par cette caractéristique, il occupe une place importante dans de nombreux secteurs. L’ozone se transforme en oxygène, sa matière première, sans laisser de résidu.
L’ozone est une molécule triatomique non linéaire. Il possède 2 liaisons oxygène de même longueur (1278°A) et un angle de liaison moyen de 1160°49.
L’ozone est un gaz très réactif, il peut être irritant et toxique même à faible concentration. Lorsque l’ozone est inhalé pendant une longue période, il produit des symptômes tels qu’une irritation des muqueuses suivie de maux de tête. Bien que nous ne disposions pas d’informations complètes sur les problèmes causés par une exposition prolongée à l’ozone, une diminution de la capacité pulmonaire et des troubles pulmonaires ont été signalés lors d’expérimentations animales.
L’organisation de la santé des employés (OSHA – Occupational Safety and Health Administration) exige que des mesures supplémentaires soient prises si la concentration d’ozone dépasse 0,1 ppm. La limite de 0,1 ppm est la limite de 8 heures de travail par jour pendant 5 jours, aux Pays-Bas, la limite est de 0,06 ppm et non de 0,1. En cas d’exposition n’excédant pas 15 minutes, la limite acceptable est de 0,3 ppm. L’OSHA a fixé une limite de 0,2 ppm pour les expositions jusqu’à 2 heures. Le seuil de discrimination pour l’odeur d’ozone est d’environ 0,02 ppm.
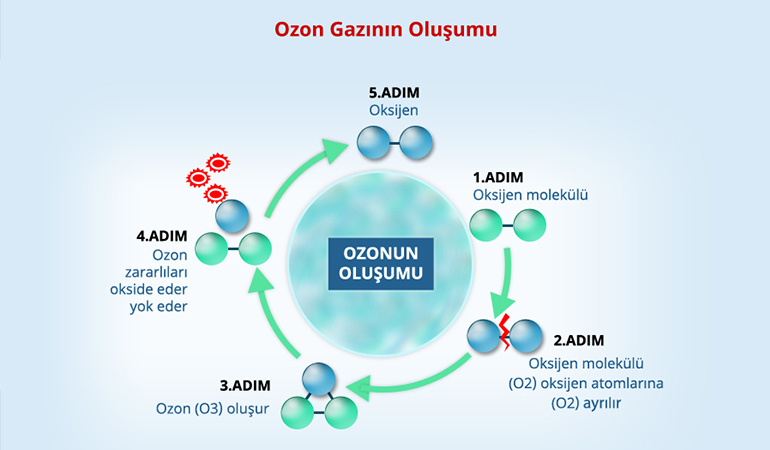
La base de la formation de l’ozone est basée sur la formation de radicaux d’oxygène atomique. Ces radicaux réagissent ensuite avec l’oxygène moléculaire pour former de l’ozone. Par conséquent, tous les processus qui convertissent l’oxygène moléculaire en radicaux oxygène sont des réactions potentielles de production d’ozone. Les énergies qui rendent cela possible sont les énergies quantiques des électrons ou des photons. Comme cela peut se produire dans des environnements naturels, des électrons peuvent être obtenus à partir de systèmes de décharge corona à haute tension, de sources chimionucléaires et de processus électrolytiques, et l’énergie quantique photonique appropriée peut être obtenue avec des rayons ultraviolets inférieurs à 200 nm et des rayons y.
Sous l’effet du rayonnement ultraviolet à haute énergie du soleil, la molécule d’oxygène O2 dans l’atmosphère est décomposée et l’oxygène libre se transforme en atomes d’O2. Plus tard, les atomes d’oxygène libres O se combinent avec la molécule d’oxygène sous l’effet du rayonnement ultraviolet pour former la molécule d’ozone O3.
L’ozone est également formé par la décharge électrique à haute tension qui se produit lors de la foudre. Un parfum frais et propre est perçu après chaque éclair et averse. Cette odeur est l’odeur d’ozone formée dans l’air. Industriellement, la première des deux principales méthodes de production d’ozone est l’utilisation de l’ultraviolet à 185 nm, la seconde est la méthode diélectrique dite Corona Discharge, qui a en elle-même différentes applications.
Dans le procédé de production d’ozone avec l’utilisation d’ultraviolets, une lampe produisant une lumière UV de 185 nm est utilisée. Lors du passage de l’air autour de la lampe UV, les molécules d’oxygène sont décomposées en atomes d’oxygène sous l’effet des UV. Comme les atomes d’oxygène formés ne sont pas stables, ils se combinent avec des molécules d’oxygène pour former de l’ozone.
La méthode Corona Discharge CD est une décharge électrique caractérisée par corona. Elle se produit par ionisation du fluide autour du conducteur lorsque le champ électrique est suffisamment fort. Les conditions ici ne doivent pas permettre la formation de courts-circuits ou d’arcs. C’est la partie diélectrique qui fournit cela. La charge électrique est répartie sur la surface diélectrique, formant la couronne. Une atmosphère de plasma se forme à la suite de l’ionisation et les ions transportent la charge vers des régions à plus faible potentiel. Lors de la formation de la couronne, de la lumière, de la chaleur et du son sont libérés.
La forme de l’électrode, la qualité du gaz et la plage de décharge sont des paramètres efficaces. Avec la méthode CD, de la chaleur est libérée lors de la production d’ozone et cette chaleur doit être évacuée du générateur. Il existe des applications où le tube à décharge est refroidi avec de l’eau ou de l’air pour évacuer la chaleur. Lorsque les deux méthodes sont comparées, on peut dire que la méthode CD est plus avantageuse que la méthode UV en termes de longévité, de concentration plus élevée d’ozone dans les petites tailles et de coûts d’exploitation. Il est très important que l’air soufflé ne soit pas humide dans les unités CD.
L’ozone peut être décrit comme un composé chimique formé par la combinaison de 3 atomes d’oxygène. Il a un parfum impressionnant. Il est incolore.
Il existe sous forme d’atome d’oxygène, d’oxygène et d’ozone dans l’atmosphère. Lorsque la molécule d’oxygène, qui se compose de deux atomes d’oxygène, spécifiés comme O2, est exposée à une haute tension, elle se sépare et se combine avec la molécule d’oxygène pour former de l’ozone (O3), qui est formé de 3 atomes. L’ozone est un gaz instable. L’ozone est formé par une puissance électrique élevée causée par la foudre par temps de pluie et se fait sentir en émettant un parfum frais. Le gaz ozone entoure le sommet de l’atmosphère, filtre les rayons ultraviolets du soleil et les envoie dans le monde. Le gaz ozone rend le ciel bleu.
La couche d’ozone est très importante pour la vie sur terre. Les substances contenant des chlorofluorocarbures endommagent la couche d’ozone, l’amenant à s’amincir ou à se perforer. Ces substances sont des dérivés chlorés, des mousses de polystyrène, des aérosols et des aérosols.
Il n’est pas possible de stocker l’ozone car il se dissout à nouveau à température ambiante et se transforme en oxygène. Il doit être produit où et quand il est utilisé. Le gaz ozone étant une molécule instable, son pouvoir d’oxydation est très élevé.

