[iSpeechWebReader textID=’contentid’]
Ozon Nedir? Nasıl Oluşur?
Ozonun CAS numarası 10028-15-6’dır. Ozon organik ve inorganik bileşiklerle birçok kimyasal reaksiyona girebilen kuvvetli bir oksidandır. Ozonun oksidasyon potansiyeli bilinen birçok kimyasaldan daha yüksektir. Yaygın olarak kullanılan hidrojen peroksidin oksidasyon potansiyeli 1,77 eV iken, ozon 2,07 eV ile florinden 3,06 eV ve hidroksil radikallerinden 2, 80 eV ile sonra gelmektedir. Oksidasyon potansiyeli oldukça yüksek olan ozon aynı zamanda etkin bir sterilitandır. Bu özelliğinden dolayı birçok sektörde önemli bir yer tutmaktadır. Ozon kalıntı bırakmadan hammaddesi olan oksijene dönüşür.
Ozon, lineer olmayan triatomik bir moleküldür. Eşit uzunlukta (1,278 °A) 2 oksijen bağına ve 1160 49’luk ortalama bağ açısına sahiptir.
Ozon son derece reaktif bir gazdır, düşük konsantrasyonlarda bile tahriş edici ve toksik etki gösterebilir. Ozon uzun süre teneffüs edildiğinde mukoz membranların tahrişi ve ardından baş ağrısı gibi semptomlar oluşturur. Ozona daha uzun süreli maruz kalma durumlarının oluşturacağı sorunlar hakkında tam bilgi sahibi olunmasa da hayvanlar üzerinde yapılan deneylerde akciğer kapasitesinde azalma ve akciğer rahatsızlıkları rapor edilmiştir.
Çalışan sağlığı örgütü ise (OSHA -Occupational Safety and Health Administration) ozon konsantrasyonunun 0,1 ppm’in üzerine çıkması durumunda ilave önlemler alınmasını istemektedir. 0,1 ppm limiti 5 günlük günde 8 saat çalışma için limittir, Hollanda’da 0,1 değil 0,06 ppm limit kabul edilmiştir. 15 dakikayı geçmeyen maruz kalma durumlarında kabul edilebilir limit 0,3 ppm’dir. OSHA 2 saate kadar olan maruz kalmalar için limiti 0,2 ppm olarak kabul etmiştir. Ozonun kokusunun ayırt edilme eşiği yaklaşık 0,02 ppm seviyesindedir.
Ozonun oluşmasının temeli ara atomik oksijen radikallerinin oluşmasına dayanmaktadır. Oluşan bu radikaller daha sonra moleküler oksijen ile reaksiyona girerek ozonu oluşturmaktadırlar. Bundan dolayı moleküler oksijeni oksijen radikaline dönüştüren bütün işlemler potansiyel ozon üretim reaksiyonlarıdır. Bunu mümkün kılan enerjiler ise elektron veya foton kuantum enerjileridir. Bu durum doğal ortamlarda gerçekleşebileceği gibi elektronlar yüksek voltajlı Corona Discharge sistemlerinden, kemonükleer kaynaklardan ve elektrolitik işlemlerden elde edilebilmekte uygun foton kuantum enerjisi ise 200 nm altındaki ultraviyole ışınları ile ve y-ışınlarıyla elde edilebilmektedir.
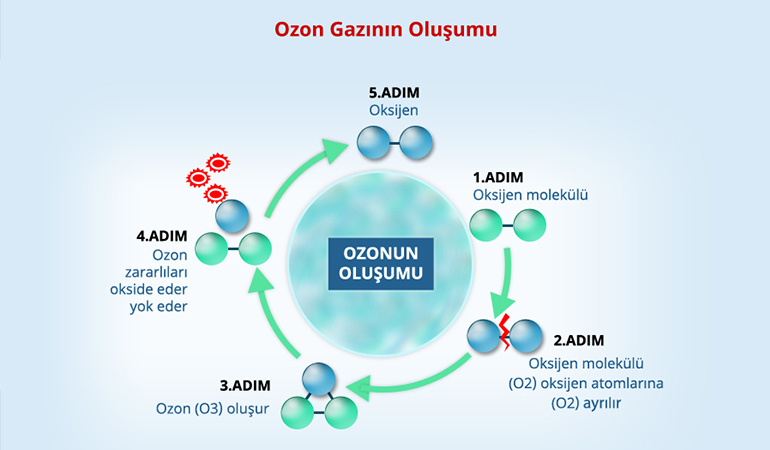
Güneşten gelen yüksek enerjili ultraviyole radyasyonunun etkisiyle atmosferdeki oksijen molekülü O2 parçalanarak, serbest oksijen O2 atomu haline dönüşmektedir. Daha sonra serbest haldeki oksijen atomları O yine ultraviyole radyasyonunun etkisiyle oksijen molekülüyle O2 birleşerek ozon molekülünü O3 oluşturmaktadırlar.
Ozonun yıldırım sırasında oluşan yüksek voltajlı elektrik boşalımı ile de oluşumu gerçekleşmektedir. Her yıldırım ve sağanak sonrasında taze ve temiz bir koku fark edilir. Bu koku havada oluşan ozonun kokusudur. Endüstriyel olarak ozon üretimi için başlıca iki metottan birincisi 185 nm de ultraviyole kullanımı, ikincisi Corona Discharge olarak bilinen ve kendi içerisinde farklı uygulamaları bulunan dielektrik metodudur.
Ultraviyole kullanımı ile ozon üretimi yönteminde 185 nm UV ışık üreten bir lamba kullanılır. UV lambanın etrafından hava geçişi esnasında UV etkisi ile oksijen molekülleri oksijen atomlarına bölünür. Oluşan oksijen atomları stabil olmadıklarından oksijen molekülleri ile birleşerek ozonu oluştururlar.
Corona Discharge CD yöntemi, korona ile karakterize edilen bir elektrik deşarjıdır. Elektrik alanı yeterince güçlü olduğunda iletkenin etrafındaki akışkanın iyonizasyonu ile gerçekleşir. Burada şartlar kısa devre ya da ark oluşumuna izin vermemelidir. Bunu sağlayan dielektrik kısımdır. Elektrik yükü dielektrik yüzeyine dağılarak koronayı oluşturur. İyonizasyon sonucu bir plazma atmosferi oluşmakta ve iyonlar yükü daha düşük potansiyele sahip bölgelere taşımaktadır. Korona oluşumu sırasında ışık, ısı ve ses açığa çıkmaktadır.
Elektrodun şekli, gazın kalitesi ve deşarj aralığı etkili parametrelerdir. CD yöntemiyle ozon üretimi sırasında ısı açığa çıkmaktadır ve bu ısının jeneratörden uzaklaştırılması gerekmektedir. Isının uzaklaştırılması için deşarj tüpünün su ile ya da hava ile soğutulduğu uygulamalar vardır. İki metod karşılaştırıldığında CD metodunun uzun ömürlü olması, küçük boyutlarda daha yüksek konsantrasyonda ozon üretimi ve işletme maliyetleri açısından UV metoduna göre daha avantajlı olduğu söylenebilir. CD ünitelerinde besleme havasının nemli olmaması çok önemlidir.
Ozon, 3 adet oksijen atomunun birleşerek meydana getirdiği kimyasal bir bileşik olarak tarif edilebilir. Etkileyici bir kokusu vardır. Renksizdir.
Atmosferde oksijen atomu, oksijen ve ozon olarak bulunur. O2 olarak belirtilen iki adet oksijen atomundan meydana gelen oksijen molekülü yüksek gerilime maruz kaldığı zaman ayrılarak oksijen molekülü ile birleşerek 3 atomun meydana getirdiği (O3) ozon oluşur. Ozon kararsız bir gazdır. Ozon yağmurlu havalarda yıldırımlar sonucu oluşan yüksek elektrik gücüyle oluşur ve fresh bir koku yayarak kendini hissettirir. Ozon gazı atmosferin en üst kısmını çepeçevre kuşatarak güneşin ultraviole ışınlarını filtre eder ve dünyaya gönderir. Ozon gazı gökyüzünün mavi görünmesini sağlar.
Ozon tabakası dünyadaki yaşam için çok önemlidir. Kloroflorokarbon içeren maddeler ozon tabakasına zarar vererek incelmesine veya delinmesine sebep olmaktadır. Bu maddeler klor türevleri, polistren köpükler, sprey ve airesollerdir.
Ozon oda sıcaklığında tekrar çözülerek oksijene dönüştüğünden depolanması mümkün değildir. Kullanıldığı yerde ve zamanda üretilmesi gerekir. Ozon gazı kararsız bir molekül olması nedeniyle oksidasyon gücü çok yüksektir.
| Ozon diğer adıyla | Triatomik oksijen veya aktif oksijen |
| Ozon tabakasının ağırlığı | 3.29×109 ton |
| Molekül formülü | O3 |
| Bileşenleri | Oksijen Atomu |
| Molekül ağırlığı | 48,998 gr |
| Sudaki çözünürlüğü | 1,09 g/L – 00C |
| Kaynama derecesi | -192,5 0C |
| Kritik sıcaklık değeri | -111,9 0C |
| Kritik basınç değeri | -12,1 0C |
| Donma noktası | 0,57 g/L – 200C |
| Isı kapasitesi | 54,6 atm – gaz |
| Buharlaşma ısısı | 33,3 j/g.mol0C, -1730 C |
| Yükseltgenme potansiyeli | 15,19kj/mol,-1120 C / 2,07 V (asidik), -1,24V |
| Absorbsiyon dalga boyu | 2537Angström – bazik |
| Renk -146 0C | Açık mavi sıvı halde |
| Renk – 220 0C | Koyu mavi kristal halde |
| Renk + 0C | Renksiz |
| Koku | Keskin fresh |
| Yoğunluk | 2,144 |
| Yanıcılık | Yanıcı değil |
| Maksimum ortam konsantrasyonu | 0,240 mg/m3 veya 0,05 ppm |






